Кристаллическое строение металлов и сплавов: основы и свойства
Введение в металловедение. Металлы и сплавы представляют собой фундаментальный материал в современном машиностроении. Их уникальные механические и технологические свойства, такие как прочность, пластичность и электропроводность, напрямую обусловлены особым внутренним строением. Важнейшей особенностью является возможность целенаправленного изменения этих характеристик в необходимом направлении, например, преобразование мягкого и пластичного материала в твердый и прочный. Для осознанного управления свойствами необходимо глубокое понимание основ их кристаллического строения, которое определяет поведение материала под различными воздействиями.
Атомная структура и кристаллизация. Все вещества состоят из огромного количества атомов, которые удерживаются силами межатомного сцепления, совершая при этом высокочастотные колебания вокруг положений равновесия. Ключевым фактором, определяющим свойства металлов, является взаимное расположение атомов, характер химических связей и расстояние между ними. В отличие от аморфных тел, таких как стекло или смола, где атомы расположены хаотично, в металлах они образуют строгий геометрический порядок. Эта упорядоченная структура, известная как кристалл, делает металлы кристаллическими телами, что и объясняет их специфические свойства.
Понятие кристаллической решетки. Различия между металлами обусловлены не только типом атомов, но и спецификой их пространственной организации, которая описывается с помощью концепции кристаллической решетки. Кристаллическая решетка представляет собой воображаемую трехмерную сетку, состоящую из повторяющихся элементарных ячеек, в узлах которых располагаются атомы, условно изображаемые в виде шариков. Основными типами решеток с плотной упаковкой атомов являются кубическая объемно-центрированная (ОЦК), кубическая гранецентрированная (ГЦК) и гексагональная плотноупакованная (ГПУ) решетка, показанные на рис. 1.1. Каждая из этих структур определяет характерные свойства металла.
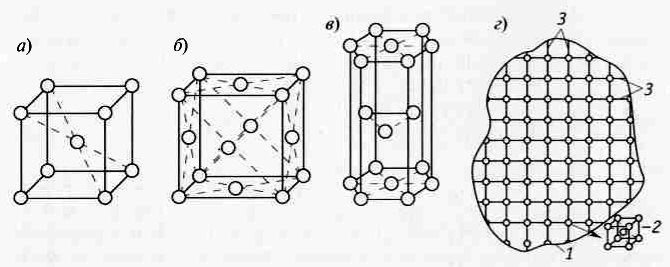
Рис. 1.1. Элементарные ячейки пространственной кристаллической решетки: а — объемно-центрированный куб; б — гранецентрированный куб; в — гексагональная ячейка; г — схема кристаллической решетки металлов: 1 — зерно — кристаллит металла; 2— элементарная ячейка; 3 — атомные плоскости
Объемно-центрированная кубическая решетка (ОЦК). В элементарной ячейке кубической объемно-центрированной решетки (ОЦК), представленной на рис. 1.1, а, атомы расположены в восьми вершинах куба и одном атоме в его центре. Данная конфигурация содержит девять атомов, что обеспечивает определенную плотность упаковки. Типичными представителями металлов, имеющих стабильную ОЦК-решетку, являются хром, вольфрам, ванадий и молибден. Важно отметить, что такие металлы, как железо, существуют в данной модификации только при определенных температурных условиях, что лежит в основе термической обработки стали.
Гранецентрированная кубическая решетка (ГЦК). Элементарная ячейка кубической гранецентрированной решетки (ГЦК), изображенная на рис. 1.1, б, характеризуется расположением атомов в вершинах куба и в центре каждой из его шести граней. Такая структура включает в себя четырнадцать атомов и обеспечивает более высокую плотность упаковки по сравнению с ОЦК-решеткой. К металлам с ГЦК-решеткой относятся медь, алюминий, никель, серебро, золото и платина. Аналогично предыдущему случаю, железо приобретает такую структуру при высоких температурах, что очень важно для его способности к легированию.
Гексагональная плотноупакованная решетка (ГПУ). Гексагональная решетка (ГПУ), схематично показанная на рис. 1.1, в, имеет ячейку в форме шестигранной призмы. Атомы расположены в двенадцати вершинах оснований, по одному атому в центре каждого основания и три атома в средней плоскости призмы, что в сумме составляет семнадцать атомов. Эта структура характерна для таких металлов, как магний, цинк, кадмий, бериллий и осмий. Металлы с ГПУ-решеткой часто демонстрируют анизотропию свойств, то есть их характеристики зависят от направления нагрузки внутри кристалла.
Полиморфизм и реальная структура металлов. Многие металлы обладают свойством полиморфизма или аллотропии, что означает способность при изменении внешних условий, например температуры, менять тип своей кристаллической решетки. Классическим примером является железо, которое при охлаждении претерпевает превращение из ГЦК-решетки в ОЦК-решетку. Аналогичным поведением обладают титан, кобальт и цирконий. Следует понимать, что элементарная ячейка является лишь минимальным повторяющимся элементом. Реальный кристаллит или зерно металла, обозначенный на рис. 1.1, г (поз. 1), состоит из гигантского количества таких периодически повторяющихся ячеек.
Влияние межатомных расстояний на свойства. Крайне важной характеристикой кристаллической структуры является расстояние между атомами в решетке или между параллельными атомными плоскостями (рис. 1.1, г, поз. 3). Это расстояние, измеряемое в нанометрах (1 нм = 10⁻⁹ м) или ангстремах (1 Å = 10⁻¹⁰ м), напрямую коррелирует с прочностью металла. Чем меньше межатомное расстояние, тем сильнее межатомные связи и, как следствие, выше прочность материала. Например, у железа это расстояние составляет 2.86 Å, у меди — 3.6 Å, а у алюминия — 4.041 Å, что и объясняет, почему железо прочнее меди, а медь прочнее алюминия.
Температурные эффекты и разрушение решетки. При нагревании металла тепловые колебания атомов вокруг узлов решетки существенно усиливаются. Это приводит к увеличению среднего расстояния между атомами и ослаблению межатомных связей. При достижении температуры, характерной для каждого конкретного металла, амплитуда колебаний становится настолько значительной, что кристаллическая структура теряет свою стабильность. Этот процесс соответствует температуре плавления, когда происходит разрушение дальнего порядка и кристаллическая решетка разрушается, переводя металл в жидкое состояние. Данное фундаментальное знание позволяет управлять процессами литья и термообработки.
Дата добавления: 2025-11-12; просмотров: 254;
