Энергетические установки с электрохимическими генераторами
Об экономичности получения электрической энергии посредством электрохимической реакции известно достаточно давно. Впервые идея создания топливных элементов была высказана английским физиком У.Р. Грове еще в 1839 году. Сам термин «топливный элемент» был впервые использован в 1889 году физиками Муидом и Лангером применительно к батареи с платиновыми электродами, а в 1894 г. немецкий физик В. Освальд впервые сформулировал идею использования топливных элементов в большой энергетике. Однако, несмотря на усилия видных ученых, в тот период не удалось достичь приемлемых характеристик топливных элементов [65], [74].
Интерес к топливным элементам вновь возрос лишь в 50-е годы прошлого столетия, когда были развернуты крупномасштабные работы по их применению в различных областях техники во многих странах мира. Однако применительно к ПЛ наиболее интенсивно они проводились в России и Германии. В 1988 году успешно прошли морские испытания российской подводной лодки проекта 613Э с электрохимическими генераторами (рис. 10.15) [67].
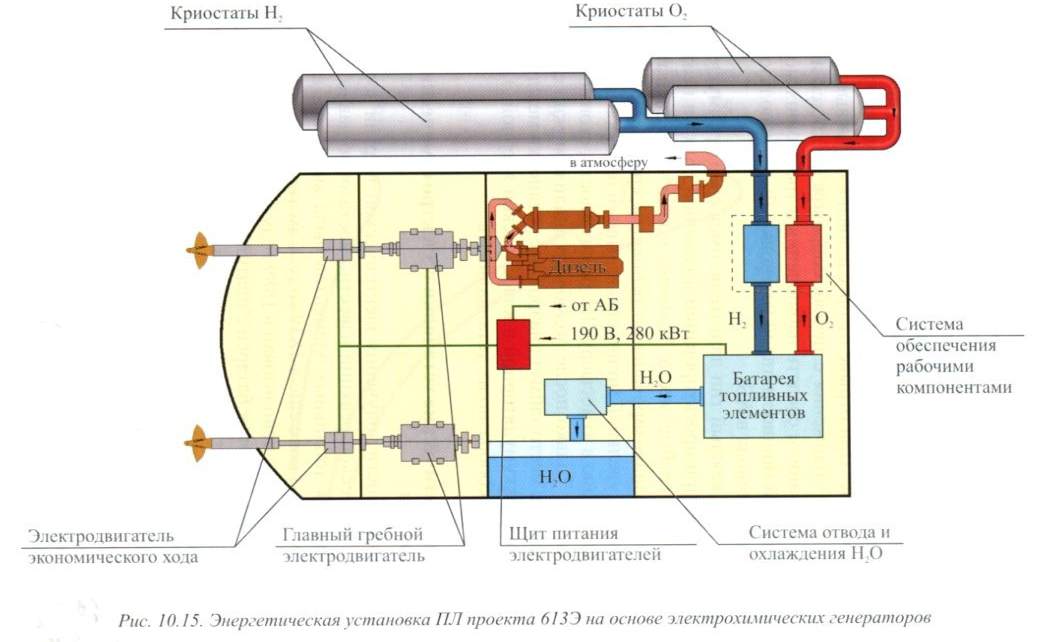
Испытания показали, что размещение такой вспомогательной установки в отдельном отсеке вызывает незначительный рост водоизмещения и, соответственно, некоторое снижение полной подводной скорости, но позволяет в несколько раз увеличить дальность плавания на экономическом ходу и в поисковом режиме без расходования энергии аккумуляторных батарей. Подобные испытания в это же время проводились и в Германии.
Перспективность данного направления развития корабельной энергетики подтверждает и тот факт, что современные неатомные подводные лодки в России и Германии проектируются с учетом установки на них вспомогательной анаэробной энергетической установки на основе топливных элементов в отдельном отсеке.
Топливный элемент представляет собой электрохимическое устройство, в котором процесс генерирования электрической энергии происходит за счет протекания реакции «окисление-восстановление» на погруженных в электролит электродах. При этом сами электроды (в отличие от аккумуляторных) в электрохимических реакциях участия не принимают, а лишь осуществляют функции накопления и передачи электрических зарядов во внешнюю цепь (электроны) и в электролит (ионы).
Генерирование энергии в топливном элементе происходит до тех пор, пока в него поступают реагенты (в простейшем случае — водород и кислород), а продукты реакции отводятся. Один топливный элемент может генерировать ток определенной плотности и напряжения. Для получения заданных выходных параметров топливные элементы соединяются в батареи.
Батарея топливных элементов, конструктивно объединенная с устройствами подачи реагентов и распределения их по элементам батареи, системами для отвода продуктов реакции, регулирования температуры и автоматики, называется электрохимическим генератором (ЭХГ).
Процесс преобразования химической энергии в электрическую в топливном элементе протекает, минуя стадию сжигания, в связи с чем теоретический КПД топливного элемента может достигать 100%.
Реально достигнутый уровень КПД лучших мировых образцов топливных элементов составляет 70...75%. Для ЭХГ характерно, что КПД практически не зависит от уровня отбираемой мощности. Удельный расход реагентов в ЭХГ лежит в пределах 0,4...0,5 кг/кВтч, что в 4-8 раз меньше, чем у тепловых машин открытого цикла. Применение ЭХГ более перспективно и по сравнению с серебряно-цинковыми аккумуляторами. Так, например, энергоустановка с ЭХГ мощностью 20...25 кВт при энергоемкости 1100 кВт-ч может иметь массу до 5000 кг и объем 3,5 м, а серебряно-цинковая аккумуляторная батарея той же энергоемкости — массу 9500...11000 кг и объем 5,6...6,4 м.
В качестве горючего в топливных элементах могут быть использованы литий (Li), натрий (Na), алюминий (А1), водород (Н2), метанол (СН3ОН), гидразин (N2H4), метан (СН4) и др. В качестве окислителя — хлор (С12), азотная кислота (HN03), сера (S), перекись водорода (Н202), кислород (02) [86].
К настоящему времени разработано большое количество топливных элементов, которые можно классифицировать по различным признакам:
— агрегатное состояние топлива: газообразное, жидкое и твердое;
— тип электролита: щелочной и кислотный;
— агрегатное состояние электролита: жидкое и твердое;
— температурный интервал, в котором работает ЭХГ — интервал низких температур (до 100 °С), средних температур (от 100 до 300 °С) и высоких температур (выше 300 °С).
Кроме того, ЭХГ подразделяются по принципу действия:
— прямого действия, когда топливо окисляется непосредственно в элементе;
— косвенного действия (топливо используется для получения продуктов, окисляющихся в ЭХГ);
— с постоянным и изменяющимся составом электродов;
— с регенерацией и без регенерации продуктов электрохимической реакции.
Обычно за основу классификации ЭХГ принимают признак агрегатного состояния реагирующих веществ, так как при таком подходе конструктивные особенности и принцип действия различаются наиболее четко.
В настоящее время наиболее освоены водородно-кислородные топливные элементы.
Удельная энергоемкость этого типа топливных элементов составляет примерно 3700 Вт-ч/кг. Существенные преимущества этих ЭХГ — их экологическая безопасность и экономичность, поскольку продуктом химической реакции является вода, которая может быть использована экипажем в качестве питьевой или для бытовых нужд, и тепло, которое можно утилизировать для обогрева. Особое значение это свойство будет иметь для ПЛ с большой дальностью плавания, позволяя уменьшить объемы цистерн пресной воды или отказаться от монтажа на борту ПЛ опреснительных установок, являющихся источником потребления электроэнергии.
ЭХГ представляет собой модульную конструкцию, что позволяет исключительно просто осуществлять ее монтаж и демонтаж в отсеке ПЛ, а также проведение регламентных работ, связанных обычно с большими трудностями вследствие сильной затесненности энергетических отсеков. Достаточно легко может быть осуществлена и замена ЭХГ при появлении новой более совершенной модификации ЭУ.
Принцип работы водородно-кислородных ЭХГ основан на следующей реакции (рис. 10.16).
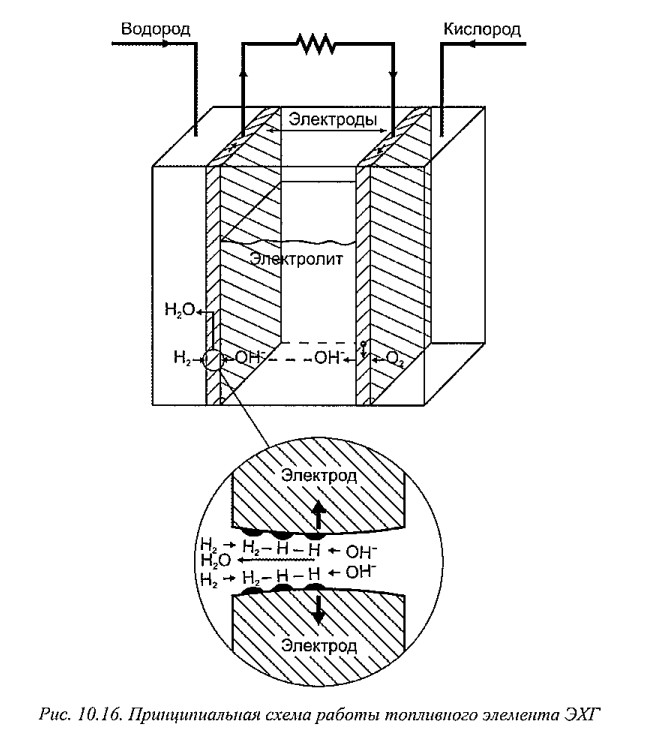
При прохождении водорода через анод его молекулы распадаются на атомы, причем в электролите, представляющем раствор едкого калия, образуются ионы гидроокисла ОН-, которые, соединяясь с атомами водорода, образуют воду и электроны. Вода поступает в электролит, а на электроде образуется отрицательный электрический потенциал. На втором электроде (катоде) происходит соединение водорода и кислорода. При этом поглощаются поступившие на электрод электроны, а из электролита извлекается вода.
Таким образом, происходит следующая реакция:
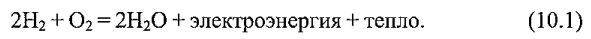
Реакция соединения водорода с кислородом, протекающая в топливных элементах, совершенно бесшумна. Единственным источником возникновения шума может оказаться насосная установка системы охлаждения, однако ее качественное исполнение и монтаж на амортизаторах гарантируют бесшумность работы всей установки. Это очень важное свойство ЭХГ, поскольку существенно повышает скрытность корабля.
Для ускорения электрохимической реакции в топливных элементах используются катализаторы (в составе материала электродов), позволяющие повысить эффективность протекания рабочего процесса в топливных элементах даже при температурах от 20 до 100 °С. В качестве катализаторов используются благородные металлы и их сплавы. Наиболее активный катализатор — платина, которая к тому же обладает высокой коррозионной стойкостью во многих средах. Широкомасштабному применению платины препятствует ее дефицитность и высокая стоимость. Для снижения стоимости топливных элементов ведется постоянный поиск более дешевых и менее дефицитных катализаторов на основе металлоорганических соединений, многокомпонентных сплавов и др.
Особую сложность в разработке ЭУ на основе ЭХГ кислородно-водородного типа вызывает проблема обеспечения надежного и безопасного хранения большого количества пожароопасных и взрывоопасных реагентов. Одно из мероприятий, уменьшающих риск, связанных с хранением кислорода и водорода, предполагает их раздельное хранение на борту ПЛ, а также хранение водорода в связанной форме (металлогидрида), которая отличается большей безопасностью по сравнению с другими способами, и кислорода в криогенной форме.
Дата добавления: 2022-01-31; просмотров: 971;
